Yhdysvaltain elintarvike- ja lääkevirasto ei ole myöntänyt, että PCR-testi Covid-19:ä varten kehitettiin käyttämällä flunssavirusta
- Artikkeli on yli kolme vuotta vanha.
- Julkaistu 28. kesäkuuta 2022 16:01
- Lukuaika: 4 minuuttia
- Teksti: Anna HOLLINGSWORTH, AFP Suomi
"FDA myöntää, että PCR testi kalibroitiin ilman eristettyä virusta vaan kalibroinnissa käytettiin tavallista flunssa virusta", sanotaan kuvakaappauksessa Twitter-päivityksestä, jota on jaettu Facebookissa yli 500 kertaa tammikuusta 2022 alkaen. "Näin on huijattu maailmaa. Kyseessä oli todellakin Plandemia."
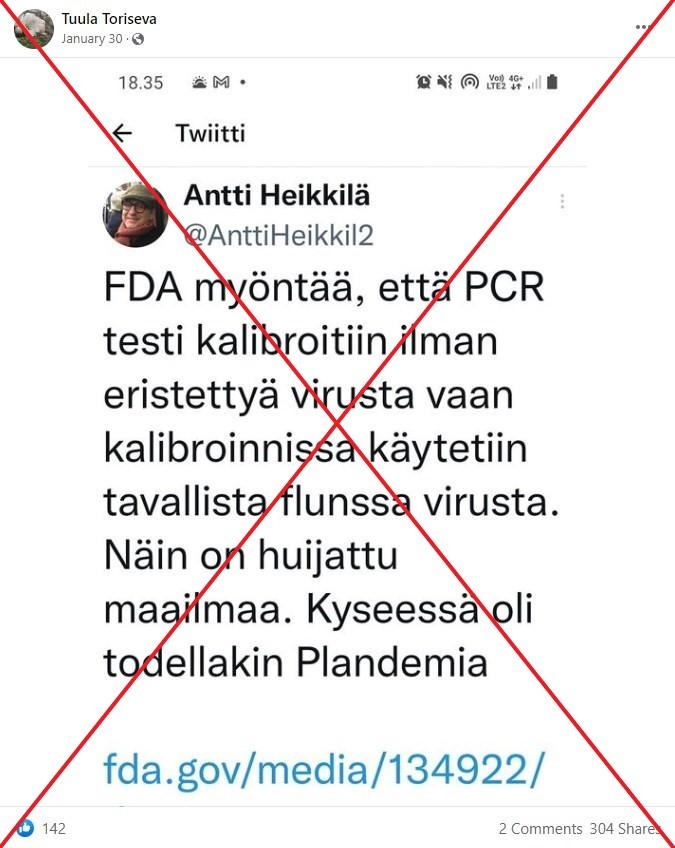
Väitteitä on jaettu esimerkiksi täällä, täällä, täällä, täällä, täällä, täällä, täällä ja täällä. Ne ilmestyivät alun perin tämän vuoden tammikuun lopussa, mutta niitä on jaettu jälleen kesäkuun puolivälin jälkeen.
Alkuperäisen twiitin julkaissut tili on poistettu ja sen mukana myös alkuperäinen twiitti. Tilin nimi ja kuva viittaavat lääkäri Antti Heikkilään, joka sai vuonna 2020 varoituksen Valviralta eli sosiaali- ja terveysalan lupa- ja valvontavirastolta potilaiden hoitamisesta yleisesti hyväksyttyjen hoitokeinojen vastaisesti ja potilasturvallisuuden vaarantamisesta sen seurauksena. Päivityksiä kommentoivat käyttäjät olettavat myös, että twiitti on häneltä.
Käyttäjien kommenttien perusteella he suhtautuvat väitteisiin vakavasti. "Miksihän mä oon törmännyt jo pariin nenäntuikkaustestimainokseen täällä Faces tällä viikolla.." yksi käyttäjä sanoi. Toinen vastasi: "Koska kusetus ja uutta paniikkia ajetaan sisään."
Useat kommentoijat ilmaisivat myös epäilyksensä rokotteita kohtaan: "Mä oon ottanut kolme rokotetta, ja oon tuuman mut että enää en ota. Ihmisiä on kuollut ihan tarpeeksi niihin rokotteisiin.. saa muistaa munkin elämää rukouksessa."
Osassa kuvakaappauksista näkyy pidempi versio twiitistä, jossa on linkki FDA:n sivuston CDC:n PCR-testin käyttöohjeeseen ("CDC 2019-Novel Coronavirus (2019-nCoV) Real-Time RT-PCR Diagnostic Panel"). Joissakin päivityksistä linkki ei näy kuvakaappauksessa, mutta se on lisätty kommenttina päivitykseen.
CDC kehitti, sai pikahyväksynnän ja aloitti kyseisen PCR-testin jakelun alkuvuodesta 2020.
Se on yksi monista FDA:n hyväksymistä PCR-testeistä. FDA listaa kaikki SARS-CoV-2:ta varten kehitetyille molekyylitesteille annetut pikahyväksynnät. 23.6.2022 tehdyllä haulla niiden joukossa oli 223 PCR-testiä.
Covid-19-tartunnan diagnosoimiseen käytetyt PCR-testit ovat saaneet osakseen useita harhaanjohtavia ja epätosia väitteitä. AFP on osoittanut vääräksi niistä useita, mukaan lukien väitteet, että PCR-testit eivät pysty erottamaan korona- ja influenssaviruksia toisistaan, että PCR-testit ovat johtaneet suureen määrään vääriä positiivisia tuloksia ja että koronavirustestit voivat johtaa kuolemaan.
AFP otti yhteyttä FDA:han ja kahteen asiantuntijaan, jotka olivat yhtä mieltä siitä, että väite, että flunssavirusta olisi käytetty yllä mainitun PCR-testin kehittämiseen, on epätosi.
Miten PCR-testi kehitettiin?
Twiitissä, josta kuvakaappaus on otettu, FDA:n käyttöohjeet esitetään todisteena väitteille PCR-testistä. AFP kuitenkin kävi käyttöohjeen läpi, eikä siinä mainita, että flunssavirusta olisi käytetty SARS-CoV-2:n, Covid-19-tautia aiheuttavan viruksen, korvikkeena.
Sen sijaan ohjeissa sanotaan: "Koska 2019-nCoV:stä ei ollut saatavilla kvantifioituja virusisolaatteja CDC:n käyttöön, kun testi kehitettiin ja tämä tutkimus tehtiin, 2019-nCoV:n RNA:n havaitsemiseen suunnitellut testit testattiin in vitro transkriptoidun täyspitkan RNA:n kuvatuilla varastoilla [--] kliinisen näytteen jäljittelemiseksi."
Asiantuntijat kertoivat AFP:lle, että synteettisen viruksen käyttäminen tartunnan saaneelta ihmiseltä otetun viruksen sijaan on yleisesti käytetty menetelmä testien kehittämisessä.
Virologian dosentti Jussi Hepojoki Helsingin yliopistolta selitti AFP:lle 27.6.2022, että virusisolaatti on potilasnäytteestä otettu ja soluviljelmässä kasvatettu virus. Hän sanoi, että kyseessä olevaa PCR-testiä varten CDC käytti kuitenkin toista menetelmää, "synteettistä RNA:ta", jota käytetään yleisesti testin herkkyyden määrittämiseen.
"Tässä tapauksessa tietysti ongelmana oli alkuun se, että viruksen RNA:ta ei ollut saatavilla", hän sanoi. "Viruksen RNA:ta on myös hankala saada niin paljon, että sen avulla pystyisi selvittämään testin herkkyyden, koska herkkyyttä määritettäessä on kyettävä mittaamaan RNA:n pitoisuus myös verrokkimenetelmällä." Hän lisäsi, että menetelmän etuna on, että ei tarvitse käsitellä mahdollisesti vaarallista patogeenia.
Kun testi on kehitetty tällä tavalla, Hepojoen mukaan seuraava askel on arvioida testin toimivuutta oikeilla näytteillä. "Potilasnäytteistä voi toki aina monistua jotain muuta, joten siksikin on käytettävä vastaavanlaisia näytteitä kuin joista patogeeni olisi tarkoitus lopulta osoittaa", hän sanoi.
Kliinisen virologian johtaja Matt Binnicker Rochesterin Mayo-klinikalta oli samaa mieltä. Hän kertoi AFP:lle 22.6.2022: "Aikaisin pandemiassa ei ollut olemassa kvantifioitua kontrollia SARS-CoV-2-virukselle, jota olisi voitu käyttää havaitsemisrajatutkimuksissa [toim. huom. eli sen määrittämisessä, kuinka monta viruksen genomikopiota tarvitaan, jotta testi antaa positiivisen tuloksen]. Toisin sanoen kun CDC yritti määrittää pienimmän määrän virusta, jonka heidän testinsä pystyisi havaitsemaan, heillä ei ollut saatavilla kontrollia, jossa oli tiedetty/ kvantifioitu määrä virusta." Tämän vuoksi he tekivät kopion viruksen genomista, joka kvantifioitiin ja jota käytettiin havaitsemisrajatutkimuksissa.
"Tämä on yleinen toimintapa laboratorioalalla etenkin, kun kyseessä on uusi tai harvinainen patogeeni", Binnicker lisäsi.
FDA:n lehdistövastaava Shirley Simson vahvisti tämän. "Materiaali, jota käytettiin testin analyyttiseen validitointiin edustaa SARS-CoV-2:ta, vaikka sitä ei ole eristetty kliinisestä näytteestä, ja osoittaa, että testit pystyvät havaitsemaan SARS-CoV-2:n potilasnäytteissä", hän sanoi 22.6. Hän selitti, että pandemian alussa FDA hyväksyi yli 50 testiä, jotka perustuivat keinotekoisista näytteistä saatuun aineistoon, testien saatavuuden nopeuttamiseksi, sillä "aitoja kliinisiä näytteitä ei ollut saatavilla".
Hän lisäsi, että testin kliinistä toimivuutta oikeassa elämässä arvioitiin kliinisessä tutkimuksessa, jossa analysoitiin hengitystienäytteitä potilailta, joilla epäiltiin Covid-19:ä.

Binnickerin mukaan flunssa- tai influenssavirusta ei käytetty korvaamaan SARS-CoV-2:ta. "Itse asiassa he käyttivät flunssaviruksia (esimerkiksi ihmisen koronaviruskantoja 229E, OC43, NL63 ja HKU1) ja influenssaviruksia ristireaktiivisuus- eli spesifisyyspaneelissaan ja osoittivat, että CDC:n Covid-19-testi oli negatiivinen, kun sillä testattiin näitä viruksia", hän selitti. "Tämä osoitti, että Covid-19-testi ei ole positiivinen, jos potilaalla on flunssa- tai influenssavirus, ja että se on spesifi SARS-CoV-2:lle."
Käyttöohjeet vahvistavat tämän, kuten niiden taulukossa 9 on esitetty.
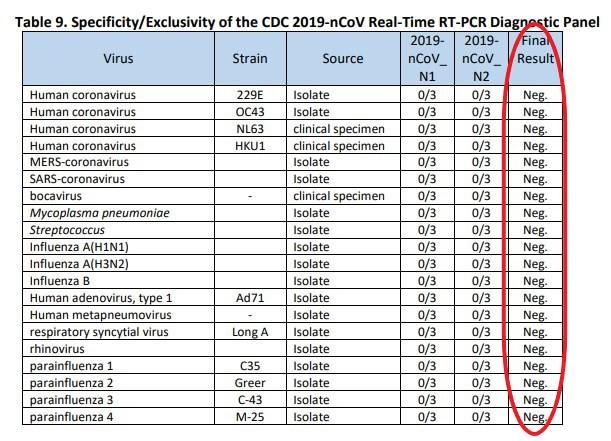
Myös Hepojoki sanoi, että koska Covid-19:n oireet muistuttavat flunssaa, on todennäköistä, että suuressa osassa testattavia näytteitä on muita tavallisia flunssaviruksia, minkä vuoksi testin kehitysvaiheessa halutaan varmistaa, etteivät muut virukset anna väärää positiivista tulosta.
Simson yhtyi tähän. "Flunssavirusta ei koskaan käytetty korvikkeena SARS-CoV-2:lle validointitutkimuksissa, joita FDA on tarkastellut lupien myöntämisen tueksi", hän sanoi. "Kaikki validointi suoritettiin käyttämällä SARS-CoV-2:ta edustavaa materiaalia."
Miksi testi vedettiin pois?
Heinäkuussa 2021 CDC ilmoitti vetävänsä pois pyyntönsä kyseisen PCR-testin pikahyväksynnästä.
Ilmoituksen aikaan levisi väitteitä, että tämä oli todiste siitä, että PCR-testit eivät pysty erottamaan Covid-19:ä ja flunssaa. AFP on kuitenkin osoittanut väitteet vääräksi täällä. CDC:n edustaja Jane Fulce selitti silloin, että päätös ei johtunut toimivuustekijöistä vaan CDC:n testin kysynnän laskusta, kun saataville tuli korkeampaa teknologiaa hyödyntäviä menetelmiä.
Tekijänoikeus © AFP 2017-2026. Sisältöjen kaupallinen käyttö vaatii tilauksen. Lue lisää täältä.
Ehdota meille faktantarkistusta.
Ota yhteyttä