Sosiaalisessa mediassa tulkitaan väärin geenitekniikkalainsäädäntöä
- Artikkeli on yli kolme vuotta vanha.
- Julkaistu 30. syyskuuta 2022 15:45
- Lukuaika: 7 minuuttia
- Teksti: Anna HOLLINGSWORTH, AFP Suomi
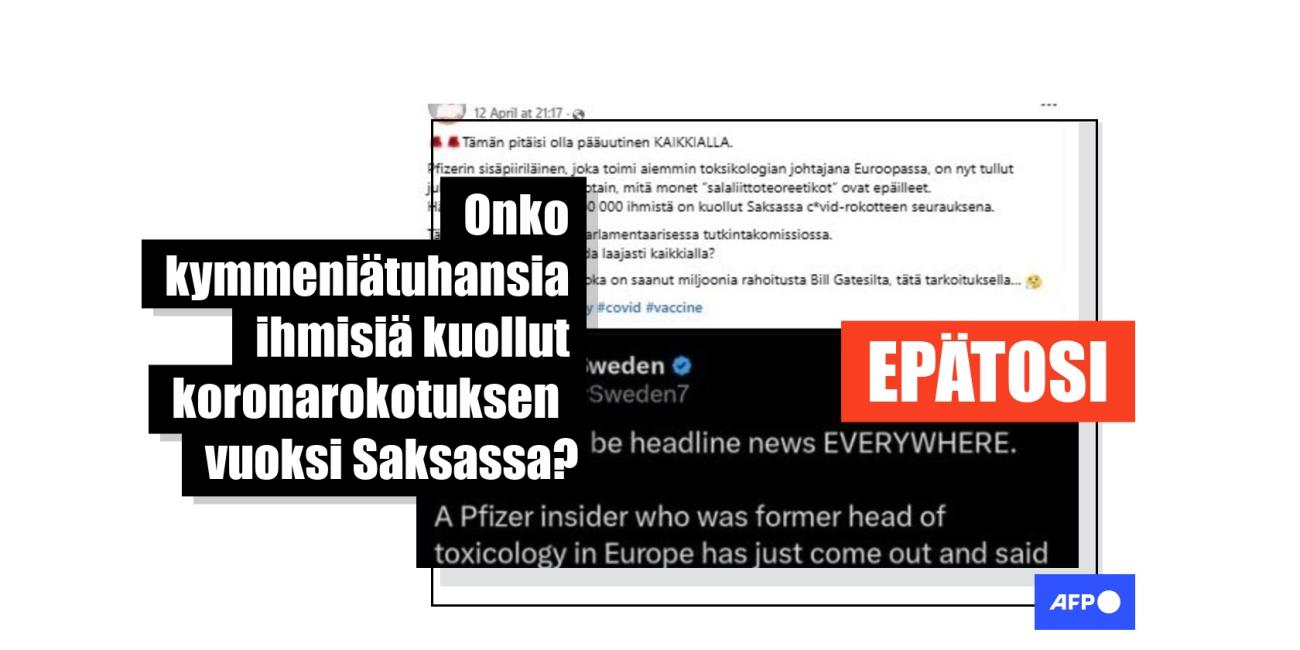
Marraskuusta 2021 lähtien sosiaalisessa mediassa kiertäneissä ja elokuussa 2022 uudelleen esiin tulleissa kuvissa väitetään, että Suomen geenitekniikkalainsäädäntö osoittaa, että koronarokotteet ovat kokeellisia ja mahdollinen "bioriski" ja että jokainen, joka saa rokotteen, osallistuu "massakenttäkokeeseen", jossa jotkut saavat plaseboa. Kuvia on jaettu yli 200 kertaa Facebookissa, Twitterissä ja Telegramissa.
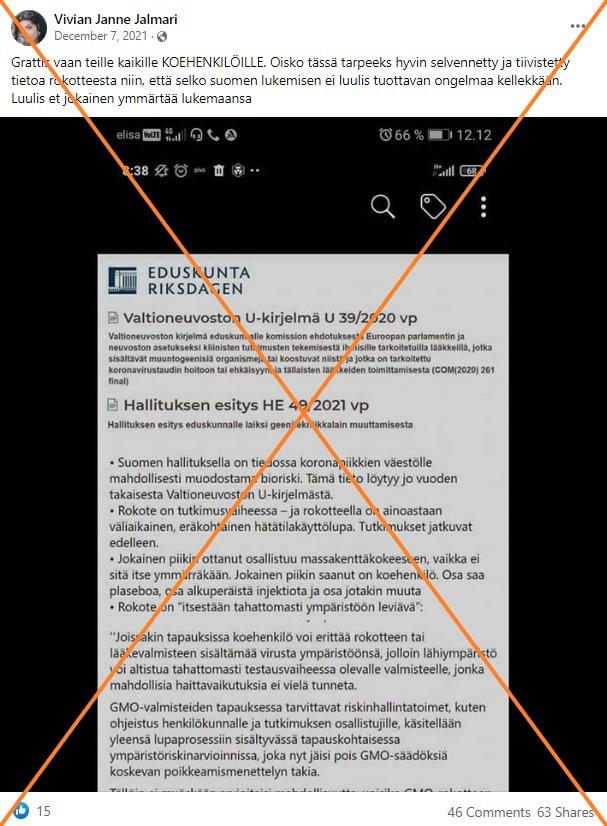
Kuvissa näkyy eduskunnan logo vasemmassa yläkulmassa sekä kahden geenitekniikkaan liittyvän eduskuntadokumentin otsikot ylhäällä. Niiden alla on ranskalaisilla viivoilla tehty listaus epätosista tai harhaanjohtavista väitteistä.
Harhaanjohtavassa kuvassa väitetään ensiksi, että Suomen hallituksella on tiedossa "koronapiikkien väestölle mahdollisesti muodostama bioriski". Toisessa kohdassa sanotaan, että rokote on "tutkimusvaiheessa" ja sillä on vain "väliaikainen, eräkohtainen hätätilakäyttölupa". Seuraavaksi väitetään, että jokainen, joka saa rokotteen, "osallistuu massakenttäkokeeseen, vaikka ei sitä itse ymmärräkään" ja että "osa saa plaseboa, osa alkuperäistä injektiota ja osa jotakin muuta". Lopuksi päivityksissä väitetään, että rokote on "itsestään tahattomasti ympäristöön leviävä".
Asiantuntijoiden ja asianomaisten viranomaisten julkisesti saatavilla olevien tietojen mukaan väitteet ovat kuitenkin epätosia tai harhaanjohtavia.
Mistä eduskuntadokumenteissa on kyse?
Ensimmäinen kuvassa mainittu dokumentti, U-kirjelmä U 39/2020, viittaa heinäkuulle 2020 päivättyyn hallituksen kirjelmään, jossa esitellään eduskunnalle Euroopan komission ehdotus Covid-19-rokotteiden ja -hoitojen kehittämisen, valmistuksen ja käyttöönoton nopeuttamiseksi. Tarkemmin ottaen ehdotuksessa esitetään, että Covid-19-rokotteiden tutkimuksilta Covid-19-pandemian aikana ei edellytettäisi tavanomaisia ympäristöriskien arviointiin ja niiden lupamenettelyihin liittyviä prosesseja, jotka koskevat muuntogeenisiä organismeja (GMO) sisältävien lääkeaineiden kliinisiä tutkimuksia. Tutkimuksen toimeksiantajan pitäisi kuitenkin toteuttaa asianmukaiset toimenpiteet minimoidakseen tutkimuslääkkeen leviämisestä ympäristöön aiheutuvat, ennakoitavissa olevat kielteiset ympäristövaikutukset.
Poikkeusmenettelyä voitaisiin soveltaa myös tapauksiin, joita varten on jo käytössä erikoismenettelyitä. Näihin kuuluvat tapaukset, joissa tuote on tarkoitettu yksittäisen potilaan hoitoon erityistarvetta varten erityisluvalla direktiivin 2001/83/EY 5. artiklan 1. kohdan mukaisesti. Menettelyä voitaisiin myös soveltaa, kun jäsenvaltio antaa luvan lääkkeen, jolla ei ole vielä myyntilupaa, jakeluun tilanteissa, joissa leviää esimerkiksi ydinsäteilyä tai haitallisia kemikaaleja. Sitä voidaan myös soveltaa tapauksissa, joissa lääke asetetaan saataville potilaille, joilla on krooninen tai muuten vakava sairaus, jota ei voida hoitaa luvallisilla lääkkeillä.
Asetus hyväksyttiin Euroopan parlamentissa heinäkuussa 2021, eli se koskee myös Suomea.
Geenitekniikan lautakunnan pääsihteeri Kirsi Törmäkangas selitti AFP:lle sähköpostitse 28.9.2022, että poikkeusmenettely ei koske GMO-rokotteiden ja -lääkevalmisteiden valmistusta eikä myyntilupaprosessia. "Valmistusta koskevat siis edelleen normaalit kansalliset lupamenettelyt, ja myyntilupaprosessissa Euroopan lääkevirasto (EMA) soveltaa samoja GMO-rokotteita ja lääkevalmisteita koskevia lupa- ja ympäristöriskinarviointimenettelyjä kuin aiemminkin", hän sanoi. Geenitekniikan lautakunta on kansallinen toimivaltainen viranomainen GMO:n käyttöä koskevissa asioissa ja toimii sosiaali- ja terveysministeriön yhteydessä.
Törmäkangas selitti myös, että koska asetus koskee vain GMO-valmisteita, se ei koske mRNA-rokotteita, sillä niissä on vain tiettyä proteiinia koodaava geenijakso. Se koskee kuitenkin AstraZenecan ja Johnson&Johnsonin rokotteita. Kuten Terveyden ja hyvinvoinnin laitos selittää sivuillaan, näissä adenovirusvektorirokotteissa koronaviruksen geeni, jonka sisältämän ohjeen avulla solut pystyvät tuottamaan koronaviruksen pintaproteiinia eli piikkiproteiinia, on siirretty osaksi vaarattoman kuljettajaviruksen perimää.
Toisessa otsikossa viitataan vuonna 2021 tehtyyn hallituksen esitykseen HE 49/2021, jossa esitetään muutosta geenitekniikkalakiin. Toukokuussa 2021 AFP osoitti vääräksi epätoden väitteen, että esitys sallii ihmisten salaisen geneettisen muokkauksen. Sen sijaan esitys perustuu EU:n yleisen elintarvikeasetuksen uudistukseen ja koskee lähinnä tietojen luottamuksellisuutta. Lisäksi GMO:lla tehtävien kenttäkokeiden yleisön kuulemisaika lyhennettäisiin 60:stä 30 päivään. Tietyissä tapauksissa kuulemista ei tarvitsisi järjestää; tämä koskee tapauksia, joissa on kyse kiireellisestä lääkinnällisestä tutkimuksesta, toimenpiteestä tai hoidosta, jonka tarkoituksena on ihmisen hengen tai terveyden turvaaminen, tai jos kuuleminen vaarantaisi tutkimuksen, toimenpiteen tai hoidon kohteena olevan henkilön yksityisyyden suojan. Esitys hyväksyttiin eduskunnassa toukokuussa 2021.
Myyntiluvan saaneet koronarokotteet eivät ole kokeellisia
Suomessa on käytössä tällä hetkellä neljä koronarokotetta, kuten sosiaali- ja terveysministeriön sivuilla selitetään: Pfizer ja BioNTechin Comirnaty, Modernan Spikevax, Johnson&Johnsonin Covid-19 Vaccine Jansen ja Novavaxin Nuvaxovoid. Lisäksi Suomessa käytettiin AstraZenecan Vaxzevriaa marraskuuhun 2021 asti.
Kaikilla rokotteilla on EMA:n myöntämä ehdollinen myyntilupa. Virasto selittää sivuillaan, että kyseistä lupaa käytetään tukemaan "lääkkeiden kehitystä vastaamaan tyydyttämättömiä lääketieteellisiä tarpeita". Sivuilla sanotaan lisäksi, että tällaisille lääkkeille voidaan antaa ehdollinen myyntilupa yleisen terveyden hyväksi "vähemmän perusteellisen kliinisen datan perusteella kuin yleensä vaaditaan, kun lääkkeen välittömän saatavuuden hyödyt ovat suuremmat verrattuna riskeihin,jotka liittyvät siihen, että lisädataa tarvitaan vielä".
EMA myönsi ehdollisen myyntiluvan Pfizerin rokotteelle (katso kohta "Key developments since authorisation") joulukuussa 2020, ja se uusittiin marraskuussa 2021; Modernan rokotteelle lupa myönnettiin tammikuussa 2021 ja uusittiin lokakuussa 2021; Johnson&Johnsonin rokotteelle lupa myönnettiin maaliskuussa 2021 ja uusittiin tammikuussa 2022; ja Novavaxille lupa myönnettiin joulukuussa 2021. Syyskuussa 2022 EMA suositteli normaalin myyntiluvan myöntämistä Pfizerin ja Modernan rokotteilla. Jutun julkaisuajankohtana 30.9. päätöstä ei ollut tehty.
Sosiaalisen median päivitykset ovat oikeassa siinä, että rokotteilla on määräaikainen myyntilupa, sillä ehdolliset myyntiluvat ovat voimassa vuoden ajan, minkä jälkeen ne voidaan uusia.
Vaikka EMA:n mukaan ehdollista myyntilupaa voidaan käyttää "mahdollistamaan lääkkeiden varhainen saatavuus käyttöä varten hätätilanteissa", se kuitenkin huomauttaa, että menettelyssä on mukana enemmän suojatoimia kuin eri maissa käytetyissä hätäkäyttöluvissa. EMA:n mukaan hätäkäyttölupa "antaa mahdollisuuden lääkkeen väliaikaiseen käyttöön tietyissä tilanteissa niin kauan, kuin hätätila on voimassa. Lääkettä ei kuitenkaan ole lisensoitu eikä sitä voida saattaa markkinoille toisin kuin (ehdollisen) myyntiluvan kohdalla".
On myös harhaanjohtavaa sanoa, että rokotteet, joille on myönnetty ehdollinen myyntilupa, ovat "kokeellisia", kuten päivityksissä väitetään. Lääkealan turvallisuus- ja kehityskeskuksen Fimean sivuilla selitetään, että "myyntiluvan saaneet rokotteet eivät ole kokeellisia rokotteita, vaikka kyseessä olisi ehdollinen myyntilupa". Fimean mukaan myös ehdollisen myyntiluvan myöntäminen vaatii, että kliiniset lääketutkimukset on tehty, ja ehdollisen ja normaali myyntiluvan saaneiden rokotteiden turvallisuutta arvioidaan samoilla kriteereillä.
AFP on tarkistanut aikaisemmin väitteitä, että koronarokotteet olisivat "kokeellisia", esimerkiksi tässä faktantarkistukselta helmikuulta 2022. Siinä riippumattomat asiantuntijat selittivät, että vaikka uutta dataa kerätään yhä henkilöiltä, jotka ovat antaneet suostumuksensa kolmannen vaiheen kliiniseen tutkimukseen tai uusiin, tiettyjä väestönryhmiä koskeviin kliinisiin tutkimuksiin osallistumiselle, tämä ei tarkoita, että väestössä yleensä rokotetut osallistuisivat tietämättään kliiniseen tutkimukseen tai että käytössä olevia rokotteita voitaisiin kuvata kokeellisiksi.
Terveyslainsäädännön professori Jérôme Peigné Pariisin yliopistosta selitti AFP:lle 7.2.2022, että "Covidin vastaiset rokotteet, joita annetaan väestölle, eivät ole kokeellisia lääkeaineita". Hän lisäsi, että "ne ovat Euroopan komission hyväksymiä rokotteita, eli niitä on luvallista myydä ja lääkäreiden tai muiden terveydenhuollon ammattilaisten on luvallista käyttää niitä kaikissa jäsenmaissa erityisesti rokotusohjelman yhteydessä. Yksittäisen henkilön suostumusta ei siksi tarvita niin kuin sitä tarvittaisiin kliinisessä tutkimuksessa". Hän lisäsi, että mikään ei estä luvan saamisen jälkeen tehtyjä kliinisiä tutkimuksia – joihin tarvitaan niihin osallistuvien henkilöiden suostumus – ja että rokotevalmistajien on suoritettava tutkimuksia myyntilupaa varten esitetyn tiedon vahvistamiseksi tai esimerkiksi aineiston ulottamiseksi nuorempiin väestönosiin.
Brysseliläisen Erasmus-sairaalan eettisen neuvoston johtaja Jean-Marie Boeynaem vahvisti tämän. Hän sanoi AFP:lle 15.2.2022, että on "normaalia", että tutkimuksia tehdään myyntiluvan saamisen jälkeen.

Suomessa vain yksi lumekontrolloitu koronarokotetutkimus
Päivityksissä väitetään myös, että jokainen, joka saa rokotteen, osallistuu "massakenttäkokeeseen", jossa osa ihmisistä saa plaseboa.
FVR:n eli Suomen rokotetutkimuksen lääketieteellinen johtaja Mika Rämet sanoi AFP:lle 21.9.2022, että väitteelle "ei ole perää". "Kaikki saavat varsinaista rokotetta", hän sanoi.
Hän selitti, että toistaiseksi ainoassa lumekontrolloidussa koronarokotetutkimuksessa Suomessa tutkitaan RNA-rokotteen turvallisuutta, siedettävyyttä ja immunogeenisuutta alle 12-vuotiailla terveillä lapsilla. Tutkimus on listattu FVR:n tutkimusarkistossa, ja se on nähtävillä myös Yhdysvaltain kansallisen lääketieteellisen kirjaston ClinicalTrials.gov-tietokannassa, jossa on tietoja tutkimuksista yli 200 maassa.
"Tutkimuksessa tarjotaan kaikille osallistujille mahdollisuutta saada varsinainen rokote sokkoutuksen purun jälkeen", Rämet sanoi. Tutkimuksessa on ClinicalTrials.govin mukaan yhteensä 10 823 osallistujaa maailmanlaajuisesti.
ClinicalTrials.gov ei listaa muita Suomessa tehtäviä, lumekontrolloituja koronarokotetutkimuksia.
Mitä päivityksissä mainittuihin eduskuntadokumentteihin tulee, hallituksen esityksessä HE 49/2021 käsitellään kenttäkokeita mutta ei mainita käynnissä olevaa koronarokotetutkimusta. Kuten mainittu yllä, U-kirjelmässä on kyse kliinisistä tutkimuksista, mutta siinä ei mainita mitään tiettyä plaseboja käyttävää tai maanlaajuista tutkimusta.
Ei todisteita, että koronarokotteet voivat levitä ympäristöön
Päivityksissä väitetään lisäksi, että hallituksella on tiedossa "koronapiikkien väestölle mahdollisesti muodostama bioriski" ja että tämä on jo ilmeistä U-kirjelmästä. Päivityksissä lisätään, että rokote on "itsestään tahattomasti ympäristöön leviävä".
Törmäkangas kuitenkin selitti, että bioriskien tunnistaminen "on aivan keskeinen asia GMO-lainsäädännössä". Hän sanoi, että GMO:hin liittyvä terveys- ja ympäristöriskien arviointi on EU:ssa "erittäin tiukka" ja edellyttää, että tunnettujen riskien lisäksi myös mahdolliset odottamattomat vaikutukset ja jopa niin kutsutut tuntemattomat tuntemattomat ("unknown unknowns") otetaan huomioon arvioinnissa. Hänen mukaansa virukset voivat mutatoitua ja vaihtaa keskenään geeniainesta rekombinaatiossa ja joissakin harvinaisissa tapauksissa villityyppiset, eli ei-GMO-, rokotevirukset voivat lisääntyä kohdeorganismissa, kuten esimerkiksi elävään virukseen perustuvissa poliovirusrokotteissa.
"Lisääntymiskykyisten GMO:jen käyttöä koskevassa riskinarvioinnissa tunnistetaan aina, ovatko tällaiset tapahtumat mahdollisia myös kyseisen GMO:n tapauksessa suunnitellussa käyttötarkoituksessa, ja jos ovat, arvioidaan niistä mahdollisesti aiheutuvat vaarat sekä haitallisten tapahtumien todennäköisyys", hän sanoi. Hän kuitenkin lisäsi, että "GMO-rokotevirusten tapauksessa haittojen toteutumisen todennäköisyys on villityyppisiin viruksiin nähden käytännössä olematon, sillä niiden lisääntymis- ja infektiokykyä on tyypillisesti heikennetty".
Mitä väitteeseen, että rokotteet voisivat levitä ympäristöön itsestään, tulee, Törmäkangas selitti, että tämä on käytännössä mahdotonta.
"Covid-19-mRNA-rokotteet eivät voi levitä itsestään ympäristöön, sillä niissä ei ole viruksen lisääntymiseen ja leviämiseen tarvittavaa koneistoa vaan vain tiettyä proteiinia koodaava geenijakso", hän sanoi.
Kokonaisen viruksen tai virusgenomin sisältävien rokotteiden kohdalla virusten lisääntymis- ja tartuttamiskykyä on heikennetty tai se on kokonaan tuhottu, hän sanoi. Viruksen leviäminen ympäristöön on teoreettisesti mahdollista, jos useita asioita toteutuisi, hän selitti: GMO-rokotteen vastaanottajan täytyisi olla infektoitunut villityyppisellä viruksella, joka on lisääntymiskykyinen ja rokoteviruksen lähisukulainen. Näiden kahden viruksen täytyisi sitten päästä lähikontaktiin vastaanottajan kudoksissa ja vaihtaa perintöainesta keskenään. Tästä olisi oltava tuloksena lisääntymiskykyinen ja tartuttamiskykyinen virus, joka pystyisi leviämään ympäristöön vastaanottajan eritteistä, mikä puolestaan vaatisi, ettei hygieniasta huolehdita.
Törmäkangas kuitenkin sanoi, että "ottaen huomioon COVID-19-rokotteiden annostelutavan (intramuskulaarinen), tuollaisen yhteisinfektion ja rekombinaation sisältävän tapahtumaketjun riski on kuitenkin käytännössä olematon".
Hän lisäsi: "Geenitekniikkadirektiivien vaatimusten mukaisesti kuitenkin myös täysin hypoteettiset tapahtumankulut joudutaan käsittelemään riskinarvioinnissa, vaikka johtopäätös olisikin, että tapahtuman todennäköisyys on nolla."
Kirjelmä siis osoittaa, että hallitus on tietoinen tutkimuksiin liittyvistä teoreettisista riskeistä yleisellä tasolla kuten riskinarviointimenetelmissä vaaditaan. Kirjelmä ei kuitenkaan koske mitään tiettyä tutkimusta, ja koronarokotteiden tapauksessa ympäristöön leviämisen riski on erittäin alhainen.
Virologian professori Ilkka Julkunen Turun yliopistosta vahvisti tämän. Hän kertoi AFP:lle 21.9., että kun kehitetään rokotetta, jossa käytetään elävää heikennettyä virusta, on teoriassa mahdollista, että rokotevirusta voi erittyä ympäristöön. Suomessa ei kuitenkaan ole testattu elävää heikennettyä virusta sisältävää koronavirusrokotetta, eikä vastaavalle koronavirusrokotteelle ole myyntilupaa Euroopassa, hän sanoi.
Mitä adenovirusvektorirokotteisiin tulee, ne sisältävät elävän viruksen, "mutta se ei lisäänny ihmisen elimistössä eikä sen siten tulisi erittyä rokotetusta ihmisestä". Julkunen lisäsi, että "ympäristöriski ja myös bioriski muille ihmisille on arvioitu hyvin vähäiseksi". Covidia vastaan kehitetyt mRNA- tai proteiinirokotteet eivät puolestaan ole infektiivisiä, minkä vuoksi "ympäristölle tai muille ihmiselle voi koitua bioriskiä".
Tekijänoikeus © AFP 2017-2026. Sisältöjen kaupallinen käyttö vaatii tilauksen. Lue lisää täältä.
Ehdota meille faktantarkistusta.
Ota yhteyttä